Fakta tentang Zeolit
Zeolit merupakan senyawa aluminosilikat terhidrasi yang memiliki kerangka struktur tiga dimensi (3D), mikroporous, dan merupakan padatan kristalin dengan kandungan utama silikon, aluminium, dan oksigen serta mengikat sejumlah tertentu molekul air di dalam porinya.
Penemuan zeolit di dunia dimulai dengan ditemukannya Stilbit pada tahun 1756 oleh seorang ilmuwan bernama A. F. Constedt. Constedt menggambarkan kekhasan mineral ini ketika berada dalam pemanasan terlihat seperti mendidih karena molekulnya kehilangan air dengan sangat cepat. Sesuai dengan sifatnya tersebut maka mineral ini diberi nama zeolit yang berasal dari kata ‘zein’ yang berarti mendidih dan ‘lithos’ yang berarti batuan.
Pada tahun 1784, Barthelemy Faujas de Saint seorang profesor geologi Perancis menemukan sebuah formulasi yang cantik hasil penelitiannya tentang zeolit yang dipublikasikan dalam bukunya “Mineralogie des Volcans”. Akhirnya berkat jasanya, pada tahun 1842 zeolit baru tersebut dinamai Faujasit.

Gambar 1. Faujas de Saint dan Faujasit
Zeolit telah dipelajari oleh para ahli mineral selama lebih dari 250 tahun. Berikut ini diberikan tahun ditemukannya mineral zeolit :

Semenjak awal tahun 1940-an, ilmuwan Union Carbide telah memulai penelitiannya untuk mensintesis zeolit dan mereka berhasil mensintesis zeolit A dan X murni pada tahun 1950, dan setelah itu banyak ditemukan zeolit sintesis jenis baru.
- [AlO4]- dan [SiO4]- saling berhubungan pada sudut-sudut tetrahedralnya membentuk Al, Si framework 3D yang berpori.
- Muatan pada framework dinetralkan dengan mengikat kation-kation monovalen atau divalen di dalam porinya.
- Memiliki kemampuan sebagai penukar kation.
- Mengikat molekul air di dalam pori-porinya.
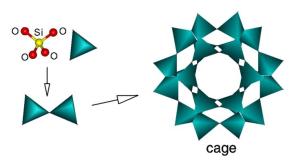
Gambar 2. Kerangka Zeolit
Karena sifat unik dari zeolit, maka zeolit banyak digunakan untuk berbagai aplikasi di industri diantaranya zeolit digunakan di industri minyak bumi sebagai ‘cracking’, di industri deterjen sebagai penukar ion, pelunak air sadah dan di industri pemurnian air, serta berbagai aplikasi lain.
Referensi
1. Curracao, Antonio., Understanding Zeolit Framework, Department of chemistry and Biochemistry, University of Bern
2. www.lenntech.com/zeolite-structure
3. Bell, R. G., What Are Zeolite?, United Kingdom, 2001
4. www.kopo.mpg.de/kopo/institut/arbeitsbereiche/scmith/research-e.htm
Air, si Cantik Yang Tersia-sia

Baru-baru ini Indonesia mengalami rentetan bencana yang berkaitan dengan air, mulai dari banjir hingga yang terakhir adalah kekeringan. Sebenarnya istilah bencana kekeringan tidak tepat juga karena kenyataannya negara kepulauan kita dikelilingi oleh air, namun tepat adanya jika kita menyebut krisis air bersih. tentu saja terjadi krisis air terutama di pulau Jawa yang berpenduduk padat dan memiliki lokasi industri demikian banyak oleh karena masih sedikit kepedulian kita terhadap zat yang cantik dan vital tersebut. Bahkan lahan tempat sumber-sumber airpun dijarah atas nama pembangunan sehingga pembangunan berwawasan lingkungan hanya tinggal menjadi istilah yang hebat namun hampa.
Bukan Sembarang Cairan
Kita yang awam mengenal air sebagai kebutuhan paling pokok, bahkan tampaknya lebih pokok daripada kebutuhan primer apapun. siapapun tak akan dapat bertahan tanpa air. sehari-hari kita berinteraksi dengan air namun alangkah miskinnya pengetahuan kita tentang air membuat kita kurang menghargainya lebih dari sekedar barang yang cair dan penting. Tak kenal maka tak sayang, maka mari kita berkenalan sedikit lebih intim dengan “water, the beautiful thing” agar semakin tumbuh kecintaan kita terhadapnya sehingga kita bisa lebih menghargainya.
Melihat air yang jernih bagaikan melihat permata berlian yang berkilauan. Sesungguhnya air yang cair itu adalah kumpulan trilyunan molekul H2O. Dalam dunia kimia dikenal H sebagai atom hidrogen dan O sebagai atom oksigen. Jadi H2O adalah satu molekul air yang mengandung satu atom oksigen dan 2 atom hidrogen. Padahal kita tahu bahwa pada tekanan atmosfer, oksigen dan hidrogen berwujud gas tapi ketika mereka bersatu saling mengikat janji bisa berubah wujudnya menjadi cair. Berkat kecerdasan kimiawan masa lalu kita dapat melakukan perhitungan begini, dalam 18 gram atau kurang lebih 18 mililiter air terkandung 6,022 x 1023 molekul H2O. Jadi, jika satu milyar adalah 10 maka bilangan tadi bermakna 602,2 ribu milyar milyar dan bilangan tersebut dikenal sebagai konstanta Avogadro. Itu baru 18 mililiter air, bayangkan jika kita meneguk segelas air atau mandi atau bahkan mengisi kolam renang, berapa banyak jumlah molekul air yang telah kita gunakan atau bahkan kita buang !!
Molekul Air yang cantik dan Istimewa
 Jika kita melihat bentuk molekul air, maka semakin terbukalah rahasia mengapa zat ini demikian istimewa. Sesungguhnya jika gas oksigen dan gas hidrogen bertemu untuk membentuk molekul air, reaksi yang terjadi sangatlah berbahaya karena bisa timbul panas yang tinggi bahkan ledakan karena oksigen adalah gas yang dibutuhkan untuk pembakaran dan hidrogen adalah gas yang mudah terbakar. Tapi untunglah Tuhan telah menyediakan air semenjak penciptaan sehingga kita tidak perlu membuat air dengan ledakan. Kurang lebih dibebaskan energi berupa panas sebesar 242 kilo Joule untuk membuat air sebanyak 18 gram dari 22,4 liter atau 2 gram gas hidrogen dan .11,2 liter atau 16 gram gas oksigen pada suhu 0 derajat Celcius dan tekanan satu atmosfer. Mari kita lihat bentuk molekul air yang berhasil diamati dengan berbagai percobaan dan perhitungan yang rumit.
Jika kita melihat bentuk molekul air, maka semakin terbukalah rahasia mengapa zat ini demikian istimewa. Sesungguhnya jika gas oksigen dan gas hidrogen bertemu untuk membentuk molekul air, reaksi yang terjadi sangatlah berbahaya karena bisa timbul panas yang tinggi bahkan ledakan karena oksigen adalah gas yang dibutuhkan untuk pembakaran dan hidrogen adalah gas yang mudah terbakar. Tapi untunglah Tuhan telah menyediakan air semenjak penciptaan sehingga kita tidak perlu membuat air dengan ledakan. Kurang lebih dibebaskan energi berupa panas sebesar 242 kilo Joule untuk membuat air sebanyak 18 gram dari 22,4 liter atau 2 gram gas hidrogen dan .11,2 liter atau 16 gram gas oksigen pada suhu 0 derajat Celcius dan tekanan satu atmosfer. Mari kita lihat bentuk molekul air yang berhasil diamati dengan berbagai percobaan dan perhitungan yang rumit.
Bentuk molekul air tersebut dan terutama sifat elektroniknya menjadikan air memiliki sifat fisika dan kimia yang fantastis. Apakah sifat elektronik itu ? Dalam pemahaman kimia dan fisika, semua sifat-sifat atom dan molekul ditentukan oleh perangai dan keadaan elektron yang mengelilingi inti atom. Ternyata alam mengajarkan kita lebih banyak lagi tentang berbagi dan bekerja sama. Ikatan yang terjadi antara dua atom hidrogen dan satu atom oksigen menjadi satu molekul air disebut ikatan kovalen. Yaitu ikatan antar atom yang terjadi karena setiap atom menyumbangkan elektron yang dimiliki untuk saling berpasangan dan digunakan bersama membentuk satu ikatan. Namun, karena oksigen memiliki kelebihan pasangan elektron, maka elektron yang tidak membentuk ikatan tersebut dikatakan sebagai “pasangan elektron bebas“. Adanya elektron bebas yang bersifat sangat negatif menjauhkan kedudukannya dari dua atom hidrogen sehingga ikatan H2O membengkok sebesar 107.5 derajat. Sedangkan keadaan alamiah atom oksigen yang bersifat negatif dan atom hidrogen yang bersifat positif menimbulkan pengkutuban atau perbedaan muatan. Kedua keadaan itulah yang menjadikan molekul air bersifat polar, artinya molekul air memiliki perbedaan muatan yakni negatif pada sisi pasangan elektron bebas dan positif pada sisi atom hidrogen. Kepolaran air bisa berarti segalanya dan amatlah besar faedahnya. Kepolaranlah yang menjadikan air dapat menghantarkan arus listrik. Berkat sifat air yang polar, dia bisa melarutkan berbagai macam zat lain, misalnya darah, protein, vitamin, garam dan lain-lain. Kenyataannya, air merupakan pelarut universal yang paling ramah terhadap lingkungan. Demikian sebaliknya, air terpisah dari minyak dan lemak karena adanya perbedaan kepolaran. Coba bayangkan jika air dan minyak dapat bercampur, betapa susahnya membersihkan tumpahan minyak di laut lepas !!. Walaupun demikian, sering kali sifat air sebagai pelarut universal malah merugikan dirinya sendiri karena dia mudah sekali tercemari oleh beraneka ragam materi kimia maupun biologi sehingga sulit untuk membersihkannya lagi, apalagi ditambah dengan ketidakkepedulian kita untuk menjaga kemurniannya.
Adanya perbedaan muatan menjadikan ikatan antar molekul air sendiri cukup kuat sehingga pada suhu ruangan dia berbentuk cair, dibandingkan dengan bensin yang segera menguap. Aksi tarik menarik antara atom hidrogen di satu molekul air dengan pasangan elektron bebas pada molekul air yang lain disebut ikatan hidrogen dan oleh sebab itu diperlukan suhu 100o Celcius untuk mengubah keadaan cair menjadi uap. Air dikatakan memiliki nilai kalor spesifik yang tinggi, artinya diperlukan energi yang cukup besar untuk menjadikannya mendidih sebaliknya air dapat melepaskan panas perlahan-lahan ke lingkungan. Berkat sifat tersebut iklim di bumi tetap stabil demikian juga tubuh kita memiliki suhu yang konstan karena kurang lebih 70% permukaan bumi dan 60% tubuh mahluk hidup terdiri dari air.
Begitu banyak keistimewaan air sehingga manfaatnya pun demikian luas mencakup berbagai aspek seperti kimia, fisika, biologi hingga agama, budaya, seni, bahkan ekonomi dan politik. Jika penelitian terakhir menunjukkan banyak situ-situ di sekitar Jakarta mulai menghilang itu berarti telah terjadi kesalahan dalam pengelolaan lingkungan. Bukan tidak mungkin suatu saat nanti Jakarta akan benar-benar kehabisan mata air dan harus memproduksi air bersih dengan teknologi yang lebih mahal dan lebih rumit akibat kelalaian kita bersama. Sungguh, air yang cantik dan sangat penting dalam kehidupan kita itu memang materi yang paling melimpah di bumi. Air diciptakan dan dicurahkan bukan berarti untuk disia-siakan, maka sekarang saatnya untuk kita lebih menghargai air sebagai ciptaan Tuhan yang paling indah.
Fosfor Putih pada Penyerangan Israel ke Gaza

Penyerangan Israel ke Gaza baru-baru ini, Januari 2009, menambah pelajaran berharga pada kita semua. Seperti pisau, pada suatu saat dan situasi biasa merupakan alat yang bermanfaat (misal: untk menyiapkan makanan bagi keluarga kita) namun pada saat dan situasi yang berbeda bisa menjadi alat yang merusak dan bahkan bisa membunuh. Demikian juga bahan kimia, ditangan Israel fosfor putih yang sebenarnya bermanfaat telah menjadi alat/bahan yang efektif untuk memerangi Palestina.
Mengapa demikian?
Fosfor putih pada dasarnya sangat berguna untuk kehidupan. Dalam industri banyak digunakan untuk memproduksi asam fosfat dan senyawa kimia lain yang berguna pada pembuatan pupuk, bahan tambahan makanan, farmasi, pengolahan air, pakan ternak, senyawa pembersih dan perapuhan logam anti karat. Dalam konsentrasi kecil fosfor putih digunakan pada kembang api. Tetapi karena sifat kimia fisiknya yaitu ketika berada di udara terbuka dengan mudah akan terbakar dan mengeluarkan asap, maka sifat ini kemudian dimanfaatkan oleh militer (misal: Israel dan Amerika) untuk menghalau musuh-musuhnya.
Apakah sebenarnya fosfor putih itu dan bagaimana sifat-sifatnya?
Fosfor adalah unsur nonlogam bersimbol P dengan nomor atom 15 dan berat atom 30,97376. Biasanya digunakan dalam pembuatan asam fosfat, perunggu, suar, teknik perapian, korek api, racun tikus, dll. Alotrop fosfor ada beberapa: fosfor putih (kuning), fosfor merah, dan fosfor hitam yang masing-masing memiliki sifat kimia fisik yang berbeda.
Fosfor putih (white phosphorus) adalah alat pembakar yang memproduksi asap dan suar yang berasal dari allotrop unsur fosfor. Material ini merupakan padatan putih (tak berwarna atau kuning) beracun yang bersifat seperti malam, lembut, berbau seperti bawang putih, meleleh pada 44,5 oC, larut dalam karbon disulfida, tidak larut dalam air dan alkohol. Unsur ini bereaksi secara cepat dengan oksigen sehingga akan terbakar dengan sendirinya di udara. Dikenal juga sebagai fosfor kuning.
Alotrop sendiri adalah keadaan dimana suatu unsur dapat memiliki lebih dari satu bentuk atau struktur yang stabil biasanya pada daerah temperatur yang berbeda, contohnya adalah bentuk kristal yang berbeda dari karbon, grafit, dan intan. Dikenal juga dengan istilah alotriomorfisme, alotropisme.
Apa yang terjadi ketika manusia terpapar dengan fosfor putih?
Meskipun belum ada penelitian yang mendalam tentang efek fosfor putih pada kesehatan manusia, tetapi dari beberapa fakta yang terjadi pada pekerja yang berhubungan dengan unsur ini menunjukkan bahwa jika terpapar dengan fosfor putih dapat menyebabkan terbakar, iritasi,kerusakan hati, ginjal, paru-paru atau tulang, yang terparah adalah kematian.
Badan-badan yang berwenang di Amerika (NIOSH, OSHA, ACGIH) telah menentukan ambang batas paparan di tempat kerja selama 8 jam kerja adalah 0,1 miligram fosfor putih per meter kubik udara (http://www.atsdr.cdc.gov/tfacts103.html).
Jadi bisa dibayangkan apa yang terjadi di Palestina saat ini. Sungguh sangat disayangkan sesuatu yang sesungguhnya bermanfaat menjadi bersifat merusak ketika berada di tangan yang salah.
Satu hal yang harus menjadi bahan pemikiran adalah bahwa penggunaan fosfor putih dalam perang tidak dilarang. Hal ini karena statusnya dalam Konvensi Senjata Kimia; Chemical Weapons Convention (CWC); bahan ini tidak termasuk dalam list senjata kimia. Kalau melihat akibatnya dalam perang itu hal ini patutlah dipertanyakan. Why………………..???
Dekomposisi Hidrogen dari Air Dengan Natrium

Hidrogen menawarkan keuntungan sebagai sumber energi yang ramah lingkungan dan tanpa polusi. Hidrogen paling banyak diproduksi dari gas alam (48%), dan merupakan elemen paling ringan di dunia (berat atom = 1 g/mol), sehingga kemampuan difusinya sangat tinggi. Bisa juga digunakan sebagai bahan bakar reaktor fusi (masih tahap pengembangan), dan sebagai sumber bahan baku pembuatan HidroCarbon (BBM Sintetis). Salah satu kendala untuk produksi hidrogen adalah sumber gas alam sendiri adalah sumber energi yang tak dapat diperbaharui, cadangannya pun semakin menipis, dan harganya terus naik, apakah ada cara lain untuk mendapatkan hidrogen? Bagaimana mendapatkannya? Banyak caranya, diantaranya dengan elektrolisis air, namun kendalanya adalah biaya yang sangat mahal. Apakah ada cara lainnya… Ada, yaitu dengan Natrium/Sodium.
Natrium banyak tersedia dan melimpah jumlahnya di lautan Bumi sebagai NaCl (garam), Natrium adalah elemen yang sangat reaktif, biaya produksi natrium pada tahun 1997 adalah US$ 0.30/kg - US$0.45/kg, cukup murah. Pada kondisi standar, logam natrium jika direaksikan dengan air akan menghasilkan gas hidrogen dengan reaksi sebagai berikut:
2Na + 2H2O → 2NaOH + H2 …………………………..(1) Eksotermal
2H2 + O2 → 2H2O ……………………………….(2) Autoignition
Reaksi tersebut bersifat eksotermal yang menghasilkan panas, sehingga gas hidrogen secara otomatis terbakar, ini disebabkan karena gas hidrogen mengalami proses autoignition akibat perpindahan panas dari reaksi ke lingkungan. Yang menjadi pertanyaan adalah, apakah mungkin gas hidrogen dari reaksi ini dipanen? Jawabnya mungkin…
Gas Hidrogen memiliki Flammability Limit dengan kisaran volume 4 - 75 % di udara, dan memiliki Autoignition Point pada suhu 585 0C, reaksi pembakaran selalu membutuhkan oksigen, begitu juga dengan Hidrogen, dengan reaksi sebagai berikut:
2H2 + O2 → 2H2O ……………………………….(3)
Proses Autoignition Hidrogen pada reaksi Natrium dengan Air dapat dicegah dengan cara menyingkirkan oksigen pada sistem tertutup sehingga Flammability Limit dan Autoignition tidak berlaku, bagaimana caranya? Dengan metode hampa dan gas inert (Nitrogen).
Nitrogen memiliki titik didih pada -195.79 0C, pada kondisi cair nitrogen memilki suhu dibawah - 195.79 0C. Pelepasan gas nitrogen secara cepat kedalam sistem tertutup dapat menggantikan posisi oksigen. Pada kondisi standar, suhu kamar 25 0C, Nitrogen cair akan mendidih dengan sangat cepat, tuangkan nitrogen cair (suhu < - 196 0C) dari tabungnya kedalam wadah logam (yang bersuhu + 25 0C), maka nitrogen cair akan mendidih dengan sangat cepat namun tidak lama, bisa ditambahkan air agar lebih lama mendidihnya, gas inilah yang akan dimanfaatkan untuk menyingkirkan oksigen.
Pada saat kondisi sistem (tertutup) telah dihampakan (vacum), segera isi dengan gas nitrogen, kemudian reaksikan natrium dengan air, akan menghasilkan gas hidrogen dan natrium hidroksida (produk samping), karena berada pada kondisi inert, reaksi autoignition hidrogen bisa dicegah, sekalipun efek eksotermall terus terjadi. Karena berat atom hidrogen = 1, maka hidrogen akan selalu mengisi ruang yang paling atas, difusifitasnya pun sangat cepat, tidak lupa juga hidrogen harus melewati kondensor agar suhunya turun (akibat proses eksotermal), setelah dingin bisa dikumpulkan dan dikompresi lalu hidrogen siap dipanen, sehingga proses ini memungkinkan untuk dilakukan.
Bisa juga untuk menurunkan efek eksotermalnya, sebelum direaksikan natrium dicelupkan dulu ke nitrogen cair ( < - 195.79 0C), baru kemudian direaksikan dengan air, diharapkan efek eksotermalnya sedikit berkurang karena suhu natrium yang berada pada kisaran - 195 0C.
Selain itu produk sampingnya yang berupa NaOH memiliki nilai jual juga, sehingga proses ini sangat menguntungkan.
Resiko Toksik pada Air Botol?

Peneliti geokimia di Jerman mengklaim bahwa botol-botol plastik secara terus menerus melepaskan unsur antimonium (Sb) ke dalam air minum.
Tim peneliti yang dipimpin oleh Bill Shotyk di University of Heidelberg menguji air-air yang dikemas dalam botol di daerah yang sama di Canada.
Air yang dikemas dalam botol polietilen tereftalat (PET) mengandung hingga 375 ppt antimonium, sedangkan air dalam botol polipropilen mengandung hanya 8,2 ppt antimonium. Tiga bulan kemudian, air dalam botol PET mengandung hingga 626 ppt antimonium. PET dibuat dengan menggunakan katalis antimonium.
Kelompok peneliti Shotyk menguji air tanah yang berasal dari daerah yang sama di Canada, dengan menggunakan alat penganalisis biji es yang sangat sensitif. Kadar antimonium yang mereka temukan sangat rendah (2 ppt). Laporan-laporan terdahulu melaporkan kandungan rata-rata 300 ppt.
"Saya tidak yakin berapa banyak lab di luar sana yang benar-benar bisa mengukur berapa banyak antimonium yang terdapat dalam air tanah, kebanyakan orang memiliki batas deteksi yang jauh di atas nilai alami pada air tanah," kata Shotyk.
Kadar antimonium dalam air botol yang diteliti ini lebih rendah dari kadar pengkontaminasi maksimum yang dianjurkan oleh EPA Amerika Serikat, yakni 6 bagian per juta. Shotyk lebih khawatir bahwa antimonium terus menerus terlepas ke dalam air dalam kemasan botol. "Yang ingin saya tunjukkan bukan bahwa air-air botol ini terkontaminasi oleh antimonium," kata dia, "tetapi hal yang penting adalah bahwa antimonium secara terus menerus dilepaskan dari botol ke dalam air".
David Coggan, seorang ahli epidemiologi dari unit epidemiologi lingkungan MRC di Southampton, Inggris, menunjukkan sikap yang berhati-hati dalam menanggapi temuan ini. Hasil yang ditunjukkan oleh Shotyk masih memerlukan penyelidikan lebih lanjut sebelum implikasi kesehatannya bisa dibahas, kata dia, sebagian karena masih sedikit yang diketahui tentang toksisitas antimonium. "Penting untuk memikirkan tentang rentang dosis berapa yang akan didapatkan oleh orang yang meminum air tersebut," kata Coggan. Meski demikian, Shotyk yang menemukan temuan ini tidak lagi meminum air yang dikemas dalam botol-botol PET.
Air Berperan Sebagai Katalis Dalam Proses Peledakan

Bahan mentah yang paling berlimpah di bumi telah diketahui dapat memperlihatkan sebagai bahan kimia yang tidak semestinya ketika diletakkan pada kondisi yang sangat ekstrim.
Baru-baru ini, para ilmuwan di Laboratorium Nasional Awrence Livermore telah memperlihatkan sesuatu hasil penelitian yang menarik bahwa air, jika diletakkan pada pada suhu kamar panas, berperan sebagai katalisasi complex dalam reaksi bahan peledak yang tak terbayangkan sebelumnya. Sebelumnya katalis hanya dapat berupa platinum dan enzim tapi untuk air sangat jarang sekali.
Letusan berasal dari bahan peledak yang terbuat dari oksigen dan hydrogen yang dapat memproduksi air pada suhu 1000 derajat dan bertekanan lebih dari 100,000 atm.
Dengan menggunakan prinsip terdahulu dari stimulasi atomistic peledakan bahan bakar tingkat tinggi PETN (penta erythritol tetranitrate) tim ilmuwan ini telah menemukan hal tersebut di air, ketika atom hydrogen bekerja sebagai reduktor dan hydrogen sebagai oksidator, atom-atom ini bertindak sebagai kelompok dinamik yang membawa oksigen selama reaksi berlangsung.
Dalam simulasi molekul dinamik dengan menggunakan Blue Gene super komputer Laboratorium , Wu dan Larry Fried, Lin Ynag, Nir Goldman dan Sorin Bastea telah menemukan atom hydrogen (H) dan hidroksida (OH) di air yang membawa oksigen dari gudang nitrogen menuju bahan bakar karbon (dengan suhu bertemperatur antara 3000-4200 Kelvin). Pada kondisi seperti itu, air bekerja sebagai produk akhir dan katalis kimia yang sangat penting.
Untuk molekul berkekuatan bahan peledak tinggi yang terbuat dari karbon, nitrogen, oksigen dan hydrogen seperti PETN, 3 produk utama gas nya adalah air, karbon dioksida dan molekul nitrogen.
Tim ilmuwan ini telah menemukan bahwa nitrogen kehilangan oksigen lebih banyak daripada hydrogen dan karbon walaupun konsentrasi air telah mencapai keseimbangan.
” Air merupakan bagian dari energi. Mekanisme katalis secara keseluruhan berbeda dengan komposisi sebelumnya yang hanya sebagai produk akhir ” kata Wu. Penemuan terbaru ini bermaksud agar para ilmuwan mempelajari keadaan yang terjadi di planet Uranus dan Neptunus. Dimana airnya yang mempunyai bentuk yang luar biasa.
Material Kaca Berkarakter Ganda : Cermin dan Transparan

Pada tahun 1996, sekelompok peneliti di Belanda menemukan sejenis material yang dapat di ubah-ubah dari keadaan transparan ke reflektif (cermin) dan atau sebaliknya dengan mengekspos material termaksud dalam gas hidrogen. Peneliti menemukan bahwa film tipis dari metal yang dinamakan yttrium dan lanthanum , dengan bantuan hidrogen, kemudian membentuk senyawa hidrida metalik yang bersifat mengkilap. Jika ditambah lebih banyak lagi hidrogen ia menjadi transparan. Transformasi dari transparan ke reflektif (cermin) dapat dilakukan dengan memompa hidrogen diatas film pada tekanan yang berbeda.
Agar perubahan dari kaca transparan ke cermin dapat dilakukan dengan baik maka peralatannya perlu dioperasikan secara elektris, dan komponen materialnya harus berbentuk benda padat.
Rob Armitage dan rekan-rekannya dari the Lawrence Berkeley National Laboratory, di California, AS menjelaskan cara kerja alat yang dioperasikan dengan tombol . Cermin terdiri dari enam lapisan yang kompleks dan tersimpan pada gelas atau kaca. Lapisan tersebut merupakan logam campuran magnesium dan gadolinium, yang yang dapat bersifat reflektif apabila mengandung sedikit atau tanpa hidrogen tetapi akan menjadi transparan dengan kandungan hidrogen yang tinggi.
Atom hidrogen yang mempengaruhi fase transisi atau fase pergantian dari transparan ke cermin tersebut diatas disimpan dalam lapisan tungsten trioxide yang memiliki muatan positif . Jika lapisan magnesium-gadolinium diberi muatan relatif negatif; terhadap film tungsten trioxide, hidrogen didorong kedalam logam campuran, dan akan menjadi terang. Pada waktu yang bersamaan tungsten trioxide , yang berwarna biru, pudar warnanya ketika hidrogen terbuang. Diantara dua lapisan terdapat ; film tipis palladium yang dapat ditembus oleh hidrogen dan dapat membantu mentransformasikan atom hidrogen bermuatan positif kedalam salah status yang netral , sehingga dapat dikombinasikan dengan logam campuran pada saat membentuk senyawa hidrida. Pada saat voltase atau tegangan berbalik, hidrogen kembali ke lapisan tungsten trioxide, dan logam campuran berubah menjadi cermin kembali.
Para peneliti mengatakan bahwa cermin benda padat yang diuraikan tersebut diatas dapat stabil dalam keadaan transparan untuk beberapa jam. Secara prinsip film logam campuran dapat berubah dari transparan ke cermin hanya dalam beberapa menit saja sehingga cukup prospektif untuk diterapkan.
Cermin dengan tombol listrik serupa di atas mungkin akan berguna bagi teknologi komunikasi optik. Sebagai contoh, pancaran cahaya yang memuat informasi data tertulis dalam pulsa optikal mungkin dapat disalurkan atau dialirkan kembali dari satu serat optik ke serat yang lainnya dengan mentransformasikan kaca jendela transparan ke kaca jendela yang dapat bersifat reflektif serupa cermin.
Merubah batuan besi menjadi bahan anti kanker

Ada banyak bahan kimia yang sedang dikembangkan oleh para peneliti saat ini karena prospeknya untuk di gunakan sebagai zat anti kanker. Fokus terbesar adalah penelitian terhadap senyawa-senyawa dari tumbuhan baik darat maupun tumbuhan laut yang bersifat aktif terhadap sel kanker. Senyawa-senyawa ini pada umunya merupakan turunan flavanoid. Sayangnya, untuk menemukan senyawa aktif tersebut dibutuhkan waktu yang agak lama karena harus diekstrak dari berbagai sumber, dikarakterisasi, diuji aktivitasnya kemudian baru disintesis untuk memperbanyak jumlahnya.
yang dihubungkan oleh jembatan oksigen. Struktur seperti ini menghasilkan resultan momen magnet yang nyata serta kemampuan untuk transfer elektron ke ion tetangga secara simultan.

Struktur kristal magnetit dan salah satu foto SEM partikel magnetit
Agar magnetit tepat sasaran saat menyerang sel kanker, biasanya zat ini dimasukkan ke dalam tubuh bersama-sama dengan obat-obatan tertentu. Setelah magnetit diserap oleh sel kanker, maka tubuh pasien diberi medan magnet seragam dari luar dalam rentangan frekuensi yang tidak membahayakan (noninvasive). Momen magnet dari magnetit nanokristal dalam tubuh akan menjadi searah mengikuti arah momen medan luar sampai pada suatu titik dimana dia tidak lagi terpengaruh (kejenuhan magnetisasi). Ketika medan luar dihilangkan pada kondisi ini, momen magnet magnetit akan kembali secara perlahan-lahan ke kondisi awalnya. Peristiwa ini disebut relaksasi magnetik dan selalu menghasilkan panas sebagai akibat perubahan energi. Panas yang dihasilkan dalam sel kanker tersebut tidak berbahaya bagi manusia tapi sangat mematikan bagi sel kanker karena dia terkena secara langsung sehingga menyebabkan kematian sel kanker tersebut (sel kanker mati pada suhu 43°C).
Banyak metoda telah dikembangkan untuk mensintesis magnetit agar memiliki struktur nanokristal. Ini merupakan syarat utama agar bisa digunakan sebagai bahan anti kanker karena jika magnetit memiliki struktur nanokristal dia akan memperlihatkan sifat superparamagentik serta mudah diserap ke dalam sel. Metoda tersebut antara lain dekomposisi kimia, transfer fasa , sonolisis, dan hidrotermal. Sayangnya semua metoda yang ada masih menggunakan prekursor berupa bahan kimia murni yang harganya relatif mahal dan seringkali memerlukan atmosfir nitrogen dalam prosesnya.
Baru-baru ini saya dibawah bimbingan Dr. Syukri Arief, M.Eng berhasil mensintesis magnetit nanokristal secara langsung dari batuan besi yang banyak terdapat di Sumatera Barat tanpa memerlukan atmosfer inert. Batuan besi tersebut diproses secara hidrotermal sederhana sampai menghasilkan magnetit dengan kekristalan yang tinggi dan bersifat superparamagnetik. Idenya berawal dari usaha untuk meningkatkan nilai ekonomis batuan besi di beberapa kabupaten yang ada di sumatera barat. Selama ini batuan besi ditambang oleh perusahaan swasta untuk kemudian dijual mentah dengan harga murah ke Cina dan India. Tidak jarang kedua negara tersebut menjual kembali hasil olahan batuan tersebut berupa besi baja ke negara kita dengan harga yang lebih tinggi. Dengan adanya penelitian ini diharapkan usaha-usaha untuk pemanfaatan sumber daya tambang yang ada di Sumatera Barat akan lebih banyak lagi.
Daftar kepustakaan:
-
Yan, Aiguo;Liu, Xiaohe;Qiu Ghuanzhou;Wu, Hongyi;Yi, Ran;Zhang, Ning;Xu,Jing, Solvothermal synthesis and characterization of size-controlled Fe3O4 nanoparticles. Journal of Alloy and Compounds. (2007). In Press.
-
Gary Wulfsberg, Inorganic Chemistry, 2000, University Science Books, 691.
-
Xinchao Wei and Roger C. Viadero Jr, Synthesis of magnetite nanoparticles with ferric ion recovered from acid mine drainage: Impllications for environmental engineering, Journal of Colloids and Surfaces A: Physicochem. Eng. Aspects, 2007, 294 : 280-286.
-
Zhu,Hongliang;Yang,Deren;Luming,Zhu, Hydrothermal growth and characterization of magnetite (Fe3O4) thin films, Journal of Surface and Coatings Thecnology, 2007, 201 : 5870-5874.
Beberapa fakta seputar kaca

Kaca adalah salah satu produk industri kimia yang paling akrab dengan kehidupan kita sehari-hari. Tetapi seberapa banyakkah yang kita ketahui tentang senyawa unik ini? Inilah beberapa fakta tentang kaca.
Beberapa sifat-sifat kaca secara umum adalah:
- Padatan amorf (short range order).
- Berwujud padat tapi susunan atom-atomnya seperti pada zat cair.
- Tidak memiliki titik lebur yang pasti (ada range tertentu)
- Mempunyai viskositas cukup tinggi (lebih besar dari 1012 Pa.s)
- Transparan, tahan terhadap serangan kimia, kecuali hidrogen fluorida. Karena itulah kaca banyak dipakai untuk peralatan laboratorium.
- Efektif sebagai isolator.
- Mampu menahan vakum tetapi rapuh terhadap benturan.
Reaksi yang terjadi dalam pembuatan kaca secara ringkas adalah sebagai berikut:
Na2CO3 + aSiO2 ? Na2O.aSiO2 + CO2
CaCO3 + bSiO2 ? CaO.bSiO2 + CO2
Na2SO4 + cSiO2 + C ? Na2O.cSiO2 + SO2 + SO2 + CO

Kuarsa (SiO2), salah satu bentuk polimorfi silika
Secara umum, kaca komersial dapat dikelompokkan menjadi beberapa golongan:
- Silika lebur. Silika lebur atau silika vitreo dibuat melalui pirolisis silikon tetraklorida pada suhu tinggi, atau dari peleburan kuarsa atau pasir murni. Secara salah kaprah, kaca ini sering disebut kaca kuarsa (quartz glass). Kaca ini mempunyai ciri-ciri nilai ekspansi rendah dan titik pelunakan tinggi. Karena itu, kaca ini mempunyai ketahanan termal lebih tinggi daripada kaca lain. Kaca ini juga sangat transparan terhadap radiasi ultraviolet. Kaca jenis inilah yang sering digunakan sebagai kuvet untuk spektrometer UV-Visible yang harganya sekitar dua jutaan per kuvet.
- Alkali silikat. Alkali silikat adalah satu-satunya kaca dua komponen yang secara komersial, penting. Untuk membuatnya, pasir dan soda dilebur bersama-sama, dan hasilnya disebut Natrium silikat. Larutan silikat soda juga dikenal sebagai kaca larut air (water soluble glass) banyak dipakai sebagai adhesif dalam pembuatan kotak-kotak karton gelombang serta memberi sifat tahan api.
- Kaca soda gamping. Kaca soda gamping (soda-lime glass) merupakan 95 persen dari semua kaca yang dihasilkan. Kaca ini digunakan untuk membuat segala macam bejana, kaca lembaran, jendela mobil dan barang pecah belah.
- Kaca timbal. Dengan menggunakan oksida timbal sebagai pengganti kalsium dalam campuran kaca cair, didapatlah kaca timbal (lead glass). Kaca ini sangat penting dalam bidang optik, karena mempunyai indeks refraksi dan dispersi yang tinggi. Kandungan timbalnya bisa mencapai 82% (densitas 8,0, indeks bias 2,2). Kandungan timbal inilah yang memberikan kecemerlangan pada “kaca potong” (cut glass). Kaca ini juga digunakan dalam jumlah besar untuk membuat bola lampu, lampu reklame neon, radiotron, terutama karena kaca ini mempunyai tahanan (resistance) listrik tinggi. Kaca ini juga cocok dipakai sebagai perisai radiasi nuklir.
- Kaca borosilikat. Kaca borosilikat biasanya mengandung 10 sampai 20% B2O3, 80% sampai 87% silika, dan kurang dari 10% Na2O. Kaca jenis ini mempunyai koefisien ekspansi termal rendah, lebih tahan terhadap kejutan dan mempunyai stabilitas kimia tinggi, serta tahanan listrik tinggi. Perabot laboratorium yang dibuat dari kaca ini dikenal dengan nama dagang pyrex. Kaca borosilikat juga digunakan sebagai isolator tegangan tinggi, pipa lensa teleskop seperti misalnya lensa 500 cm di Mt. Palomer (AS).
- Kaca khusus. Kaca berwarna , bersalut, opal, translusen, kaca keselamatan,fitokrom, kaca optik dan kaca keramik semuanya termasuk kaca khusus. Komposisinya berbeda-beda tergantung pada produk akhir yang diinginkan.
- Serat kaca (fiber glass). Serat kaca dibuat dari komposisi kaca khusus, yang tahan terhadap kondisi cuaca. Kaca ini biasanya mempunyai kandungan silika sekitar 55%, dan alkali lebih rendah.
Barsounan, Michael. 1997. FUNDAMENTALS OF CERAMIC. The Mc-Graw Hill inc. Singapore.
Austin, Goerge T. 1984. SHEREVE’S CHEMICAL PROCESS INDUSTRIES.The Mc-Graw Hill inc.
Belerang: Superkonduktor yang diharapkan
Unsur belerang dapat ditemukan dalam beberapa bentuk allotropi, dua diantaranya adalah monoklinik dan rhombik belerang seperti gambar yang tertera di bawah ini.

Kanan : Rhombik belerang ; Kiri : Monoklinik Belerang
Kedua-duanya baik monoklinik dan rhombik belerang terbentuk dari delapan atom belerang yang membentuk molekul siklik.

Molekul siklik dari belerang padat (S8)
Rupa dari sulfur pada suhu dan tekanan biasa memiliki sifat isulator arus listrik. Walaupun, penelitian belerang pada tekanan tinggi menunjukkan bukti terjadinya transisi ke struktur berbeda yang merupakan fase logam (superkonduktivitas sering dikaitkan dengan perubahan struktur dari satu struktur kristal logam ke struktur logam lainnya, dimana struktur yang kedua menyimpang dari struktur sebelumnya). Elektromagnet khusus yang didasari oleh superkonduktif material digunakan secara luas di ilmu kedokteran untuk magnetik resonance imaging (MRI). Secara umum, superkonduktif material hanya menunjukkan sifat ini pada temperatur yang sangat rendah, lebih rendah daripada temperature hidrogen cair (20K).
Sifat dari belerang ini sangatlah penting karena fase logamnya memiliki suhu kritis yang sangat tinggi yang melampaui superkonduktivitas dari unsur-unsur benda padat lainnya yang telah diteliti. Lebih lanjut, suhu kritis ini meningkat dengan bertambahnya tekanan, merupakan sifat yang luarbiasa. Sebagai contoh, selenium dan telurium, yang merupakan satu golongan dengan belerang, menunjukkan sifat yang berbeda. Belum ada yang tahu bagaimana menjelaskan fenomena tersebut. Makna dari hasil penelitian tersebut adalah bahwa belerang membuka kesempatan untuk pengembanhan dari percobaan teori superkonduktivitas. Para peneliti sedang merencanakan untuk meningkatkan tekanan guna mempelajari sifat yang luarbiasa ini. [SS]
Raksa atau Merkuri, Bahaya dan Penanganannya
Berita di Kompas, 5 September 2002 kemarin menyatakan, sebagian besar sungai di Kalimantan Selatan (Kalsel), baik yang besar maupun yang kecil, terutama di tiga kabupaten/kota, yakni Tanah Laut, Kota Baru, dan Banjar, kini tercemar air raksa. Cemaran ini akibat kegiatan para penambang emas, baik oleh perorangan maupun perusahaan, yang diduga ilegal. Yang juga memprihatinkan, konsumen bisa dengan mudah membeli air raksa. Bahkan, dalam beberapa jam saja empat sampai lima ton air raksa habis diborong konsumen.Tulisan singkat ini memaparkan air raksa bahaya-bahayanya dan batas-batas standar yang ditetapkan oleh badan-badan kesehatan dan lingkungan dunia atau Amerika. Apakah raksa itu? Air raksa adalah logam yang ada secara alami, satu-satunya logam yang pada suhu kamar berwujud cair. Logam murninya berwarna keperakan, cairan tak berbau, mengkilap. Bila dipanaskan sampai suhu 357 oC air raksa akan menguap. Selain untuk kegiatan penambangan emas, logam merkuri digunakan dalam produksi gas khlor dan soda kaustik, termometer, tambal gigi, dan baterai.
Air raksa, sering disebut merkuri, dapat berada dalam berbagai senyawa. Bila bergabung dengan khlor, belerang atau oksigen merkuri akan membentuk garam yang biasanya berwujud padatan putih. Garam merkuri sering digunakan dalam krim pemutih dan krim antiseptik. Merkuri anorganik (logam dan garam merkuri) terdapat di udara dari deposit mineral, dan dari area industri. Merkuri yang ada di air dan tanah terutama berasal dari deposit alam, buangan limbah, dan aktivitas volkanik.
Merkuri dapat pula bersenyawa dengan karbon membentuk senyawa organo merkuri. Senyawa organomerkuri yang paling umum adalah metil merkuri, yang terutama dihasilkan oleh mikroorganisme (bakteri) di air dan tanah. Karena bakteri itu kemudian terikut (termakan) oleh ikan, maka di ikan cenderung konsentrasi merkurinya akan tinggi. Nah, dari buangan di sungai Kalimantan ini dapat saja dalam waktu beberapa tahun kemudian akan terakumulasi di ikan, kemudian dampaknya akan ada pada generasi berikutnya. Ingat kasus Minamata di Jepang.
Bagaimana orang dapat terkontaminasi merkuri? Ada beberapa cara: memakan ikan atau hewan air lainnya yang telah terkontaminasi metilmerkuri; terkontaminasi karena lepasnya merkuri dari penambal gigi (banyak pihak mengganggap kasus yang sangat jarang), menghirup udara yang mengandung merkuri dari tumpahan, atau limbah industri (orang-orang pekerja tambang yang tersebut dalam berita Kompas itu, penulis rasa rawan terhadap kontaminasi ini).
Efek merkuri pada kesehatan terutama berkaitan dengan sistem syaraf, yang sangat sensitif pada semua bentuk merkuri. Metilmerkuri dan uap merkuri logam lebih berbahaya dari bentuk-bentuk merkuri yang lain, sebab merkuri dalam kedua bentuk tersebut dapat lebih banyak mencapai otak. Pemaparan kadar tinggi merkuri, baik yang berbentuk logam, garam, maupunmetilmerkuri dapat merusak secara permanen otak, ginjal, maupun janin.
Pengaruhnya pada fungsi otak dapat mengakibatkan tremor, pengurangan pendengaran atau penglihatan dan pengurangan daya ingat. Pemaparan dalam waktu singkat pada kadar merkuri yang tinggi dapat mengakibatkan kerusakan paru-paru, muntah-muntah, peningkatan tekanan darah atau denyut jantung, kerusakan kulit, dan iritasi mata. Badan lingkungan di Amerika (EPA) menentukan bahwa merkuri klorida dan metilmerkuri adalah bahan karsiogenik.
Anak-anak lebih rentan daripada orang dewasa terhadap merkuri. Merkuri di ibu yang mengandung dapat mengalir ke janin yang sedang dikandungnya dan terakumulasi di sana. Juga dapat mengalir ke anak lewat susu ibu. Akibatnya, pada anak dapat berupa kerusakan otak, retardasi mental, buta, dan bisu. Bahkan, masalah pada pencernaan dan ginjal juga dapat terjadi.
Oleh karena itu, merkuri harus ditangani dengan hati-hati, dijauhkan dari anak-anak dan wanita yang sedang hamil. Standard yang ditetapkan badan-badan internasional untuk merkuri adalah sebagai berikut: di air minum 2 ppb (2 gr dalam 1.000.000.000 (satu milyar gr air atau kira-kira satu juta liter)). Di makanan laut 1 ppm (1 gram tiap 1 juta gram) atau satu gram dalam 10 ton makanan. Di udara 0,1 mg (miligram) metilmerkuri setiap 1 m3, 0,05 mg/m3 logam merkuri untuk orang-orang yang bekerja 40 jam seminggu (8 jam sehari). Nah, penulis mengira di Kalimantan, kalau benar peredarannya begitu bebas dan saya takut juga ditangani tidak semestinya batas-batas di atas pasti terlampaui.
Bisakah dites apakah para pekerja terkontaminasi merkuri? berdasarkan catatan sampel darah dan urin dari sesorang dapat digunakan untuk mengetahui hal ini. Kadang diambil juga sampel rambut untuk diketahui kadar merkurinya pula.
Mudah-mudahan pihak pemerintah daerah di Kalimantan segera turun tangan untuk mencegah bahaya yang lebih besar, yang saya yakin akan terjadi untuk semua lapisan dan akan melibatkan jumlah yang besar.
Teknologi Baru Pengolahan Air Membersihkan Air dengan Katalis
Baru-baru ini, Tim peneliti dari Hitachi mengumumkan bahwa mereka berhasil menemukan teknologi baru dalam pengolahan air. Mereka telah berhasil mengembangkanteknologi katalis untuk menguraikan zat organik yang terkandung dalam air. Katalis yang digunakan adalah katalis yang aktif setelah dikenai sinar ultraviolet. Dikatakan bahwa lebih dari 90 persen zat organik termasuk Dioksin bisa diuraikan dengan cara ini.
Kelebihan teknologi ini dibandingkan dengan teknologi yang ada selama ini adalah cukup menggunakan katalis tanpa menggunakan zat tambahan. Beaya proses ini jauh
Kelemahan dari teknologi ini adalah ambang konsentrasi polutan yang masih relatif kecil, dibawah 100 ppm. Sehingga, untuk air limbah yang memiliki tingkat konsentrasi zat organik sangat tinggi diperlukan proses pendahuluan untuk menurunkan kandungan zat organiknya.
Katalis adalah zat yang bisa mempercepat atau memacu terjadinya suatu reaksi. Dalam hal ini adalah reaksi penguraian zat organik. Untuk proses pengolahan air ini, katalis yang dipakai adalah Titan Oksida. Titan Oksida menjadi oksidator kuat setelah disinari sinar ultraviolet. Titan Oksida yang telah aktif tersebut akan mengoksidasi zat-zat organik ada.
Alat pembersih air yang dirancang oleh Hitachi memiliki bentuk yang sederhana. Yaitu berupa reaktor berbentuk silinder dengan sumber sinar ultraviolet pada bagian tengahnya. Sedangkan katalis ditempelkan pada dinding dalam silinder dengan zat perekat. Air limbah cukup dilewatkan pada reaktor silinder tersebut dan zat organik yang terkandung di dalamnya akan diuraikan oleh katalis yang di dinding silinder.
Saat ini, Indonesia sedang menghadapi masalah serius tentang air bersih. Kelihatannya kita bisa menaruh harapan pada pengembangan teknologi ini.












